特殊醫學用途配方食品注冊申請流程
1.受理機構
國家市場監督管理總局食品審評中心
2.辦理時限
1.受理:5個工作日;2.行政許可決定:20個工作日(不含技術審評、抽樣檢驗、現場核查、復審所需的時間)。
3.審批結果
1.《特殊醫學用途配方食品注冊證書》有效期限為5年。2.許可年審或年檢:無。
4.通辦范圍
注冊申請人應當為擬在我國境內生產并銷售特殊醫學用途配方食品的生產企業和擬向我國境內出口特殊醫學用途配方食品的境外生產企業。
5.結果送達
國家市場監督管理總局作出準予注冊決定的,受理機構自決定之日起10個工作日內頒發、送達特殊醫學用途配方食品注冊證書;作出不予注冊決定的,應當說明理由,受理機構自決定之日起10個工作日內發出特殊醫學用途配方食品不予注冊決定,并告知申請人享有依法申請行政復議或者提起行政訴訟的權利。
6.辦理依據
《中華人民共和國食品安全法》第八十條:特殊醫學用途配方食品應當經國務院食品藥品監督管理部門注冊。
7.申請條件
特殊醫學用途配方食品注冊申請人應當為擬在我國境內生產并銷售特殊醫學用途配方食品的生產企業和擬向我國境內出口特殊醫學用途配方食品的境外生產企業。
8.申請材料
(一)申請人在提交紙質申請材料之前,應先完成電子申請程序:申請人通過國家市場監督管理總局網站(http://www.samr.gov.cn/)或總局食品審評機構網站(www.cfe-samr.org.cn)進入特殊醫學用途配方食品注冊申請系統,按規定格式和內容填寫并打印注冊申請書。各項申請材料應逐頁或騎縫加蓋申請人公章或印章,并掃描成電子版上傳至特殊醫學用途配方食品注冊申請系統。
(二)申請人需按照《特殊醫學用途配方食品注冊申請材料項目與要求(試行)》(詳見附件1)提交紙質申請材料。
9.申請人權利和義務
(一)依據《中華人民共和國行政許可法》,申請人依法享有以下權利:1.依法取得行政許可的平等權利;2.對行政機關實施行政許可,享有陳述權、申辯權;3.依法申請行政復議或者提起行政訴訟;4.合法權益因行政機關違法實施行政許可受到損害的,有權依法要求賠償。
(二)依據《特殊醫學用途配方食品注冊管理辦法》(總局令第24號)第十條、第十七條和第十九條,申請人依法享有以下權利:1.受理機構受理或者不予受理注冊申請,應當出具加蓋國家市場監督管理總局行政許可受理專用章和注明日期的書面憑證。2.審評機構提出不予注冊建議的,應當向申請人發出擬不予注冊的書面通知。申請人對通知有異議的,向審評機構提出書面復審申請并說明復審理由。復審的內容僅限于原申請事項及申請材料。3.國家市場監督管理總局作出不予注冊決定的,應當說明理由,并告知申請人享有依法申請行政復議或者提起行政訴訟的權利。
(三)依據《中華人民共和國行政許可法》,申請人依法履行以下義務:1.對申請材料實質內容的真實性負責;2.依法開展取得行政許可的活動;3.如實向負責監督檢查的行政機關提供有關情況和材料。
(四)申請人應當按照《中華人民共和國食品安全法》及其實施條例、《特殊醫學用途配方食品注冊管理辦法》的規定履行相應義務。
10.結果名稱證書樣本
1.《特殊醫學用途配方食品注冊證書》有效期限為5年。 2.許可年審或年檢:無。
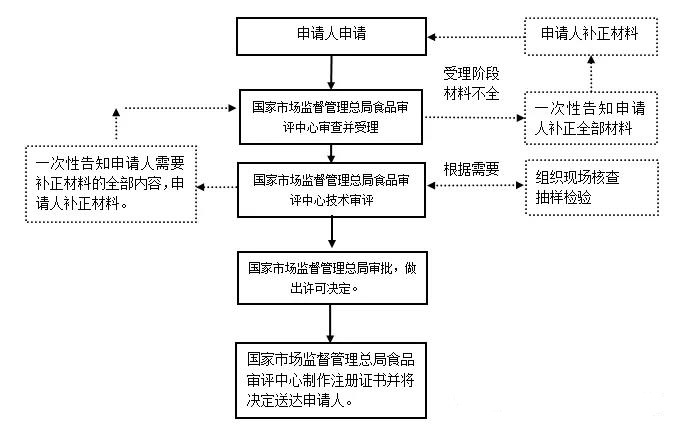
11.申請流程圖